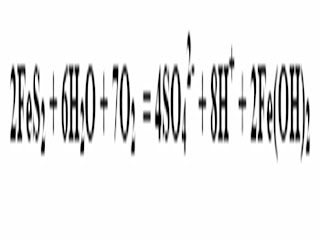Bahan Kuliah Online Fakultas Pertanian, Univ. Sriwijaya Oleh: Dr.Ir.Abdul Madjid,MS
Jumlah Pengunjung
About Me
- Dr. Ir. Abdul Madjid, MS
- Dosen Jurusan Tanah, Fak. Pertanian, Univ. Sriwijaya. Kampus Unsri Indralaya, Propinsi Sumatera Selatan
Categories
- Analisis P Tanah (6)
- Bahan Organik Tanah (1)
- Bakteri (1)
- Bakteri Pelarut Fosfat (4)
- Biologi Tanah (23)
- Cacing Tanah 0112 (10)
- Cacing Tanah 1320 (2)
- Citra Satelit (8)
- Citra Satelit Geo Eyes (1)
- Citra Satelit Lahat (1)
- Definisi Tanah (2)
- Fisika Tanah (7)
- Foto Udara (6)
- Foto Udara Kayu Agung (1)
- Foto Udara Lahat (1)
- Fungi Aspergillus 0110 (10)
- Fungi Aspergillus 1120 (10)
- Fungi Aspergillus 2130 (11)
- Fungi Aspergillus 3140 (10)
- Fungi Aspergillus 4150 (10)
- Fungi Aspergillus 5160 (10)
- Fungi Aspergillus 6168 (8)
- Fungi Mucor 0110 (9)
- Fungi Mucor 1115 (5)
- Fungi Penicillium (14)
- Fungi Penicillium 0110 (10)
- Fungi Penicillium 1120 (10)
- Fungi Rhizopus 0110 (10)
- Fungi Rhizopus 1120 (10)
- Fungi Rhizopus 2130 (10)
- Fungi Rhizopus 3137 (7)
- Fungi Rhizopus 3842 (5)
- Fungi Tanah (4)
- Ilmu Tanah (20)
- Kesesuaian Lahan (2)
- Kesuburan Tanah (21)
- Kimia Tanah (16)
- Kimia Tanah S2 (3)
- Klasifikasi Tanah (3)
- Kunci Jawaban Ujian (2)
- Mikoriza (1)
- Mikoriza 001010 (10)
- Mikoriza File (1)
- Model 3 Dimensi (1)
- Nilai Mata Kuliah (4)
- Nilai MK PUPUK (1)
- Peta (24)
- Peta Aceh Barat (1)
- Peta Belitang (1)
- Peta Cianjur (1)
- Peta Dunia (2)
- Peta Indonesia (1)
- Peta Indralaya (2)
- Peta Insert Banyuasin (1)
- Peta Insert Empat Lawang (1)
- Peta Insert Lahat (1)
- Peta Insert Linggau (1)
- Peta Insert Muara Enim (1)
- Peta Insert Muba (1)
- Peta Insert Musi Rawas (1)
- Peta Insert OI (1)
- Peta Insert OKI (1)
- Peta Insert OKU Induk (1)
- Peta Insert OKU Selatan (1)
- Peta Insert OKU Timur (1)
- Peta Insert Pagar Alam (1)
- Peta Insert Prabumulih (1)
- Peta Jabar Banten (1)
- Peta Jawa Tengah (1)
- Peta Jawa Timur (1)
- Peta Kab Lahat (3)
- Peta Kab Lebong (1)
- Peta Kab OI (3)
- Peta Kayu Agung (1)
- Peta Kudus (1)
- Peta Musi Rawas (1)
- Peta OKI (1)
- Peta OKU (1)
- Peta OKU Selatan (1)
- Peta OKU Timur (1)
- Peta Pagar Alam (1)
- Peta Papua (1)
- Peta Pulau Jawa (1)
- Peta Sumatera (1)
- Peta Sumsel (2)
- Peta Tabalong (1)
- Soal Kuis (2)
- Soal Ujian Mid Semester (3)
- Soal Ujian Semester (2)
- TOR (2)
- Tugas (1)
Blog Archive
Followers
Fasilitas Pencari Isi Blog ini:
Labels: Kimia Tanah S2
Peranan BO terhadap Sif
Komponen Penyusun Bahan Organik
Bahan organik terbentuk dari beberapa bentuk karbon organik, meliputi:
- karbon organik yang menyusun organisme hidup (makro, meso dan makro organisme),
- karbon organik yang menyusun jaringan organisme yang sudah mati tetapi belum terdekomposisi atau masih utuh,
- karbon organik yang menyusun bahan organik yang sedang dalam proses dekomposisi aktif, dan
- karbon organik yang menyusun bahan hasil dekomposisi yang bersifat lebih resisten yang disebut humus.

Perbedaan Asam Humat, Asam Fulvat dan Humin
Humus terdiri dari beberapa komponen, yaitu: asam humat, asam fulvat dan humin. Ketiga komponen penyusun humus ini dibedakan berdasarkan kelarutannya dalam asam kuat dan basa kuat. Asam fulvat bersifat larut baik dalam Basa Kuat seperti KOH atau NaOH maupun dalam asam kuat seperti HCl. Asam humat hanya larut dalam basa kuat dan tidak larut dalam asam kuat. Sedangkan humin tidak larut baik dalam basa kuat maupun dalam asam kuat.

Perbedaan Warna antara Asam Fulvat, Asam Humat dan Humin
Berdasarkan warna larutannya seperti terlihat pada gambar dibawah ini, bahwa warna dari asam fulvat berkisar warna coklat kekuning-kuningan sampai berwarna kuning cerah, sedangkan asam humat berwarna coklat gelap sampai berwarna abu-abu hitam, dan humin berwarna hitam pekat.
 Berdasarkan intensitas warna antar
Berdasarkan intensitas warna antarModel Struktur Kimia
Struktur kimia dari asam humat dan asam fulvat diilustrasikan dalam model struktur kimia berikut ini.
 Model struktur kimia dari asam humat lebih kompleks dibandingkan model struktur kimia asam fulvat.
Model struktur kimia dari asam humat lebih kompleks dibandingkan model struktur kimia asam fulvat.Komposisi Kimia
Kandungan unsur karbon (C), Hidrogen (H), Oksigen (O), Nitrogen (N) dan Sulfur (S) dari asam humat dan asam fulvat disajikan dalam tabel dibawah ini.
 Kandungan unsur karbon (C) dan Nitrogen (N) pada asam humat lebih banyak daripada asam fulvat, akan tetapi kandungan oksigen (O) pada asam fulvat lebih banyak daripada asam humat. Banyaknya kandungan oksigen tersebut berkaitan erat dengan gugus fungsional karboksilat pada asam fulvat yang lebih banyak daripada pada asam humat.
Kandungan unsur karbon (C) dan Nitrogen (N) pada asam humat lebih banyak daripada asam fulvat, akan tetapi kandungan oksigen (O) pada asam fulvat lebih banyak daripada asam humat. Banyaknya kandungan oksigen tersebut berkaitan erat dengan gugus fungsional karboksilat pada asam fulvat yang lebih banyak daripada pada asam humat.Gugus Fungsional
Kandungan gugus fungsional yang ada dalam asam humat dan asam fulvat, meliputi gugus: karboksil, fenol, alkohol, quinon, keton dan metoksil. Jumlah mol dari setiap gugus fungsional tersebut dalam setiap kg asam humat dan asam fulvat disajikan dalam tabel berikut.
 Berdasarkan tabel diatas diketahui bahwa pada asam humat lebih banyak kandungan gugus fenol daripada asam fulvat, sedangkan pada asam fulvat lebih banyak kandungan gugus karboksil daripada asam humat. Asam fulvat lebih reaktif dibandingkan asam humat.
Berdasarkan tabel diatas diketahui bahwa pada asam humat lebih banyak kandungan gugus fenol daripada asam fulvat, sedangkan pada asam fulvat lebih banyak kandungan gugus karboksil daripada asam humat. Asam fulvat lebih reaktif dibandingkan asam humat.
Labels: Bahan Organik Tanah
JURUSAN TANAH
FAKULTAS PERTANIAN
UNIVERSITAS SRIWIJAYA
SOAL UJIAN MID SEMESTER
Mata Kuliah: DASAR-DASAR ILMU TANAH
Dosen Penguji: Dr. Ir. Abdul Madjid Rohim, MS.
Waktu : 30 Menit
Jawablah soal-soal berikut pada lembar jawaban secara ringkas dan jelas.
Soal:
1. Tuliskanlah definisi tanah berdasarkan ilmu pertanian modern? (Nilai 10)
2. Gambarkanlah profil tanah yang lengkap dengan horizon-horizonnya? (Nilai 10)
3. Tuliskanlah beberapa sifat kimia tanah yang penting diketahui? (Nilai 10)
4. Tuliskanlah enam kategori pengelompokan kemasaman tanah? (Nilai 10)
5. Jelaskanlah beberapa faktor yang dapat menyebabkan terjadinya
6. Bagaimanakah cara mengatasi permasalahan kemasaman tanah yang
7. Jelaskanlah kenapa koloid tanah penting diketahui ? (Nilai 10)
8. Jelaskanlah mekanisme terjadinya muatan negatif yang bersifat tidak tergantung
9. Jelaskan pengertian dari beberapa istilah berikut:
(a) Kapasitas Tukar Kation (KTK) (Nilai 5)
(b) Kation Basa (Nilai 5)
(c) Persentase Kejenuhan Basa (%KB) (Nilai 5)
(d) Persentase Kejenuhan Aluminium (%Kej. Al) (Nilai 5)
--- 0 O 0 ---
Labels: Soal Ujian Mid Semester
1. Pengaruh Negatif dari Kemasaman Tanah terhadap Pertumbuhan Tanama,
Kemasaman Tanah
Pada daerah iklim Tropis Basah, pengasaman tanah adalah proses alamiah (natural).
Kemasaman tanah merupakan salah satu masalah utama bagi pertumbuhan tanaman.
Pada tanah bereaksi atau pH sangat masam, yaitu pH lebih rendah dari 4,5, maka dalam sistem tanah akan terjadi perubahan kimia sebagai berikut:
(a) Aluminium menjadi lebih larut dan beracun untuk tanaman.
(b) Sebagian besar hara tanaman menjadi kurang tersedia bagi tanaman, sedangkan beberapa hara mikro menjadi lebih larut dan beracun.
Masalah-masalah ini tersebar luas di daerah tropis basah yang telah mengalami pelapukan lanjut. Menurut Sanchez dan Logan (1992), bahwa sepertiga dari daerah tropis, atau 1,7miliar hektar, adalah tanah bereaksi asam dengan tingkat kelarutan aluminium cukup tinggi sehingga menjadi racun bagi tanaman.
Kita akan mengkaji beberapa penyebab pengasaman tanah dan mengetahui teknologi pengapuran untuk menetralisasi asam.
Ad 1. Pengaruh Negatif dari Kemasaman Tanah terhadap Tanaman
Kemasaman tanah dapat menyebabkan permasalahan sbb:
1. penurunan ketersediaan unsur hara bagi tanaman;
2. meningkatkan dampak unsur beracun;
3. penurunan hasil tanaman;
4. mempengaruhi fungsi penting biota tanah yang bersimbiosis dengan tanaman seperti fiksasi nitrogen oleh Rhizobium.

Konsep Kemasaman Tanah
Konsep Kemasaman Tanah adalah salah satu prinsip dasar kimia tanah yang mengindikasikan reaksi tanah. Tanah bereaksi netral jika ber pH 7,0. Jika pH tanah > 7,0 merupakan tanah bereaksi basa atau disebut tanah alkali. jika pH tanah lebih rendah dari 7,0 disebut tanah masam.
Kedua kondisi ekstrem, yaitu: terlalu asam dan terlalu basa merupakan kondisi yang sangat merugikan bagi pertumbuhan dan perkembangan tanaman. Akan tetapi, ada beberapa reaksi kimia di alam yang terjadi dalam kondisi pH netral.
Kriteria Kemasaman Tanah (pH)
Pengelompokan kemasaman tanah berbeda dengan pengelompokkan terhadap sifat kimia tanah lain, karena untuk kemasaman tanah (pH) dikelompokkan dalam enam kategori berikut:
1. Sangat Masam untuk pH tanah lebih rendah dari 4,5
2. Masam untuk pH tanah berkisar antara 4,5 s/d 5,5
3. Agak Masam untuk pH tanah berkisar antara 5,6 s/d 6,5
4. Netral untuk pH tanah berkisar antara 6,6 s/d 7,5
5. Agak Alkalis untuk pH tanah berkisar antara 7,6 s/d 8,5
6. Alkalis untuk pH tanah lebih besar dari 8,5.
Ad 2. Faktor Penyebab Terjadinya Kemasaman Tanah
Air Hujan
Ada kekhawatiran tentang hujan asam, tetapi hampir semua hujan adalah ber pH rendah (asam). Air Hujan murni yang tidak mengandung bahan pencemar pada dasarnya adalah air distilasi. Air hujan ini yang dalam kesetimbangan dengan atmosfer akan memiliki pH sekitar 5,6 karena pelarutan karbon dioksida di dalam air.
Ketika air hujan murni berada dalam kesetimbangan dengan karbon dioksida, maka konsentrasi ion hidrogen yang dihasilkan menyebabkan pH 5,6.
Respirasi Akar
Tanaman juga menghasilkan karbon dioksida karena proses respirasi akar, dan selama periode pertumbuhan aktif akar dapat menyebabkan karbon dioksida di tanah yang konsentrasinya lebih tinggi beberapa kali dari di atmosfer, sehingga terjadi peningkatan jumlah karbon dioksida terlarut dalam air tanah dan menyebabkan peningkatan keasaman tanah atau pH menjadi lebih rendah.
Pupuk
Karbon dioksida bukan satu-satunya sumber ion hidrogen dalam tanah, namun. Pada tanah yang dikelola, pupuk dapat menjadi sumber utama ion hidrogen.
Faktor Pupuk (Pupuk Amonium dan Pupuk Mono Kalsium Fosfat).
Pupuk Amonium
pupuk modern biasanya menggunakan amonium sebagai sumber nitrogen, akan tetapi oksidasi ammonium dihasilkan ion nitrat dan ion hidrogen sehingga menyebabkan pengasaman tanah.
Dengan kata lain, dua atom hidrogen dihasilkan setiap molekul ammonium teroksidasi.
Pupuk Mono Kalsium Fosfat
Monocalcium fosfat yang sering digunakan sebagai salah satu komponen pupuk juga menjadi faktor penyebab terjadinya proses pengasaman tanah (meskipun lebih rendah daripada amonium). Senyawa ini akan terhidrolisis dalam air membentuk fosfat bikalsium dan Asam fosfat
Asam fosfat terdisosiasi sangat cepat seiring dengan peningkatan pH dari 3,0 menjadi lebih dari 7.0.
Secara umum ion hidrogen (H+) ketiga tersebut akan terlarut pada pH di atas netral, sehingga tidak termasuk faktor penyebab pengasaman tanah. Akan tetapi, kedua ion hidrogen ( H+) yang sudah terlarut dalam kisaran pH tanah asam, termasuk faktor penyebab kemasaman tanah.
Ketika pupuk fosfor diberikan dalam lubang tugal, maka H3PO4 terdisosiasi dalam tanah sehingga terjadi nilai pH yang sangat rendah didekat pupuk tersebut. Tingkat keasaman ini akan secara bertahap menyebar ke dalam tanah sekitar lokasi pupuk. Menurut
Lindsay dan Stephenson (1959), nilai pH 1,5 dapat ditemukan segera di zona sekitar pupuk tersebut.
Faktor Reaksi Oksidasi yang Menghasilkan Ion Hidrogen
Semua reaksi oksidasi dalam tanah yang menghasilkan ion hidrogen dapat menyebabkan terjadinya pengasaman tanah.
Salah satu reaksi pengasaman paling efektif adalah oksidasi sulfur anorganik. Belerang biasanya digunakan jika tanah memiliki pH lebih tinggi dari yang diinginkan, sehingga diperlukan upaya penurunan pH tanah.
Misalnya, Reaksi oksidasi pirit yang terjadi pada tanah rawa yang diangkat sehingga terjadi reaksi oksidasi dari pirit tanah tersebut.
Setiap ion S dihasilkan 2 ion Hidrogen
Bahan Organik
Berbagai macam Bahan Organik juga dapat menyebabkan pengasamkan tanah. Kemampuan pengasamannya tergantung pada jenis tanaman sebagai sumber bahan organik tersebut.
Beberapa tanaman mengandung asam organik dalam jumlah yang sangat berbeda dengan tanaman lainnya. Asam organik hasil dekomposisi bahan organik menyebabkan pengasaman tanah.
Bahan organik yang berasal dari tanaman dengan kandungan basa-basa rendah juga menyebabkan terjadinya sedikit pengasaman tanah. Bahan organik yang berasal dari tanaman dengan kandungan basa-basa kurang mencukupi kebutuhan mikrobia pendekomposernya, menyebabkan mikrobia tersebut menyerap basa-basa keperluannya dari sistem tanah, sehingga basa-basa tanah seperti kalsium dan magnesium terkuras dari tanah maka menyebabkan terjadinya pengasaman tanah.
Tanaman
Pertumbuhan tanaman juga berkontribusi dalam pengasaman tanah, proses penyerapan hara utama (kalium, kalsium dan magnesium) disertai pertukaran dengan ion hidrogen sehingga menyebabkan terjadinya pengasaman tanah.
Jenis Tanaman tertentu juga mempengaruhi pengasaman tanah. Contohnya adalah tanaman Legumninosa. Selama masa pertumbuhan tanaman Leguminosa terjadi penyerapan anion dan kation dengan perbandingan yang tidak seimbang, sehingga lebih mengasamkan tanah. Tanaman leguminosa menyerap hara nitrogen dari hasil fiksasi mikrobia yang bersimbiosis dengannya. Tanaman non-leguminosa menyerap nitrogen dari sistem tanah dan penyerapan ini dalam kondisi yang seimbang dengan penyerapan kation-kation basa, sehingga lebih sedikit pertukaran dengan ion hidrogen, maka sedikit menyebabkan pengasaman tanah.
Hujan Asam
Hujan asam juga memberikan kontribusi dalam proses pengasaman tanah. Dalam sistem tanah kontribusi dari hujan asam relatif rendah dibandingkan dengan pengaruh dari pasir sesquioxida yang bersifat sangat asam yang kapasitas tukar kation sangat rendah. Akan tetapi banyak tanaman sangat peka terhadap pengaruh dari hujan asam.
Ad 3. Pengukuran pH Tanah
Reaksi tanah atau pH tanah merupakan ukuran kemasaman tanah atau kebasaan tanah.
Tanah ber pH 7 adalah tanah bereaksi netral, tanah ber pH > 7 adalah tanah bereaksi basa dan tanah ber pH lebih rendah dari 7 merupakan tanah bereaksi asam atau yang dikenal sebagai tanah masam (acid soils).
Reaksi tanah atau pH tanah dapat diukur baik dengan menggunakan pelarut air (pHw) atau bisa juga dengan menggunakan pelarut kalsium klorida (pHCa), sehingga pH hasil pengukuran akan bervariasi tergantung dari metode pelarut yang digunakan.
Sebagai aturan umum, Nilai pH yang diukur dengan pelarut kalsium klorida adalah lebih rendah 0,7 satuan unit pH daripada nilai pH yang diukur dengan pelarut air (Gambar 2).
Ketika laboratorium mengukur pH tanah Anda, maka sangatlah penting diketahui bahwa mereka menetapkan dengan menggunakan metode pelarut air atau pelarut kalsium klorida karena hasil penetapan pH dari kedua metode tersebut akan berbeda.
.
Untuk tanah yang bereaksi asam, pilihan pengelolaan yang paling praktis adalah menambahkan kapur untuk mempertahankan status pH tanah saat ini atau meningkatkan pH tanah lapisan atas (top soil)..
Labels: Kimia Tanah